El 24 de agosto de 2021, Cara Therapeutics y su socio comercial Vifor Pharma anunciaron la aprobación por la FDA de difelikefalin (KORSUVA™), el agonista del receptor opioide kappa, primero en su clase, para el tratamiento de pacientes con enfermedad renal crónica (ERC) (prurito moderado/grave asociado a hemodiálisis). Se prevé su lanzamiento en el primer trimestre de 2022. Cara y Vifor firmaron un acuerdo de licencia exclusiva para la comercialización de KORSUVA™ en Estados Unidos y acordaron venderlo a Fresenius Medical. Según este acuerdo, Cara y Vifor se reparten el 60 % y el 40 %, respectivamente, de los beneficios de las ventas no realizadas a Fresenius Medical; cada una se reparte el 50 % de los beneficios de las ventas procedentes de Fresenius Medical.
El prurito asociado a la enfermedad renal crónica (ERC-aP) es un prurito generalizado que se presenta con alta frecuencia e intensidad en pacientes con ERC sometidos a diálisis. El prurito afecta aproximadamente al 60-70 % de los pacientes en diálisis, de los cuales el 30-40 % presenta prurito moderado o grave, lo que repercute seriamente en la calidad de vida (p. ej., mala calidad del sueño) y se asocia con depresión. Hasta ahora no existía un tratamiento eficaz para el prurito relacionado con la ERC, y la aprobación de difelikefalina contribuye a cubrir esta importante necesidad médica. Esta aprobación se basa en dos ensayos clínicos fundamentales de fase III incluidos en la solicitud de autorización de comercialización: datos positivos de los ensayos KALM-1 y KALM-2 en EE. UU. y a nivel mundial, y datos de apoyo de 32 estudios clínicos adicionales, que demuestran la buena tolerancia de KORSUVA™.
Recientemente, se recibieron buenas noticias del estudio clínico de difelikefalina en Japón: el 10 de enero de 2022, Cara anunció que sus socios Maruishi Pharma y Kissey Pharma confirmaron que la inyección de difelikefalina se utiliza en Japón para el tratamiento del prurito en pacientes en hemodiálisis. Ensayos clínicos de fase III: Se alcanzó el criterio de valoración principal. 178 pacientes recibieron difelikefalina o placebo durante 6 semanas y participaron en un estudio de extensión abierto de 52 semanas. El criterio de valoración principal (cambio en la puntuación de la escala numérica del prurito) y el criterio de valoración secundario (cambio en la puntuación del prurito en la escala de gravedad de Shiratori) mejoraron significativamente con respecto al valor basal en el grupo de difelikefalina en comparación con el grupo de placebo, y fueron bien tolerados.
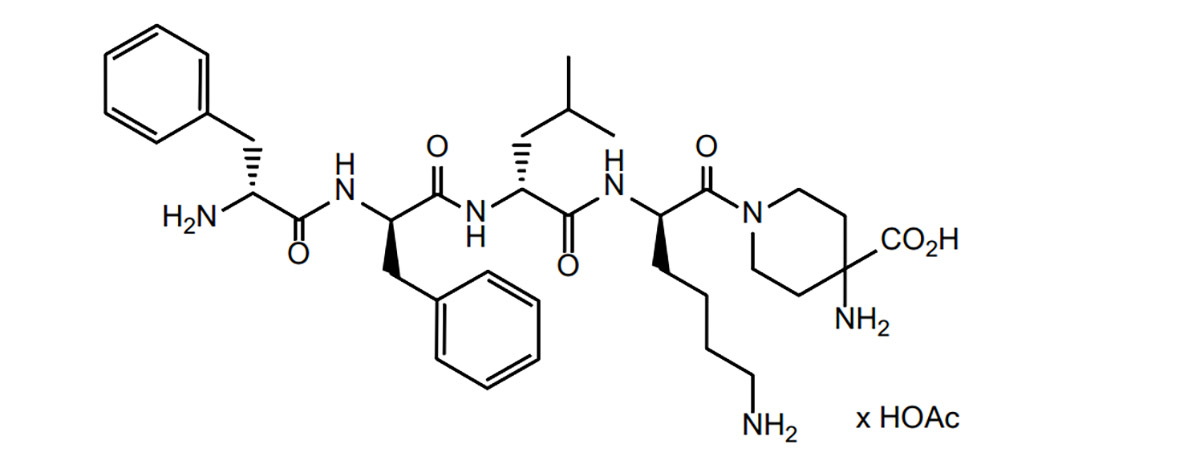
La difelikefalina es una clase de péptidos opioides. En base a esto, el Instituto de Investigación de Péptidos ha estudiado la literatura sobre péptidos opioides y ha resumido las dificultades y estrategias de estos péptidos en el desarrollo de fármacos, así como la situación actual en este campo.
Fecha de publicación: 17 de febrero de 2022